iNature
饱和脂肪酸(SFA)和不饱和脂肪酸(UFA)对健康的影响截然不同。SFA和UFA是否在肝脏中差异转运仍然难以捉摸。
2025年2月4日,苏州大学第一附属医院武艺、吴德沛、陈凤梧共同通讯在Nature communications 上在线发表题为“Differential transport pathways of saturated and unsaturated fatty acid esters in male mouse hepatocytes”的研究论文。研究发现在雄性小鼠肝内质网(ER)应激模型中,UFA而不是SFA酯的分泌受到延迟。
在蛋白二硫键异构酶(PDI)家族的13个成员中,只有PDIA1(PDI)缺乏导致肝脂肪变性和低脂血症。在PDI缺陷的雄性小鼠肝脏中,UFA酯的严重积累但分泌阻断,而SFA酯的积累和分泌保持正常。PDI催化微粒体甘油三酯转移蛋白(MTP)的氧化折叠。此外,肝细胞中的PDI缺陷会消除载脂蛋白B-100(ApoB-100)极低密度脂蛋白(VLDL)分泌,同时维持ApoB-48VLDL的部分分泌。综上所述,研究发现UFA酯的分泌是必不可少的,而SFA酯可以通过ApoB-48VLDL通过PDI-MTP非依赖性途径从肝脏中转移出去。

UFA和SFA对健康的影响截然不同。人们普遍认为,摄入大量SFA会增加血浆低密度脂蛋白(LDL)胆固醇,从而增加患心血管疾病的风险。相比之下,高消费UFA主要导致体重增加、高血糖和肝损伤。许多研究提倡用UFA代替膳食SFA以降低心血管风险。然而,一些研究表明这种膳食替代品是否适合所有人是有争议的。
许多证据表明,SFA和UFA酯在细胞中的分泌和积累可能涉及不同的机制。Abdel-Fattah等人用玉米油、猪油和棕榈仁油喂养豚鼠,发现膳食脂肪链长度和饱和度对VLDL分泌有特定影响。此外,许多研究表明,在牛卵母细胞、DAOY癌细胞、小胶质细胞、肾近端小管细胞、HepG2细胞和小鼠原代肝细胞中,UFA促进富含甘油三酯(TG)的脂滴(LD)的形成,而SFA很难转化为富含TG的LD。然而,关于UFA和SFA酯在细胞中的不同转运机制知之甚少。众所周知,内质网(ER)应激会导致肝脂肪变性,受ER应激影响的主要代谢途径被认为是脂肪生成。然而,ER应激是否影响脂质从肝脏释放的过程,以及ER应激是否与SFA和UFA的差异转运机制有关仍是未知数。
蛋白质二硫键异构酶(PDI)家族是ER中的一组硫醇氧化还原酶,可催化ER中蛋白质正确折叠所必需的翻译后二硫键交换。PDI是该家族的典型成员,在VLDL组装中起着重要作用。PDI催化ApoB-100的氧化折叠。更重要的是,PDI和MTP形成异二聚体,通过将中性脂质转移到新合成的ApoB蛋白,它在VLDL组装中起着至关重要的作用。MTP具有脂质结合和脂质转移活性,而PDI被认为可以将MTP维持在可溶性形式并通过其KDEL基序确保ER中的MTP。尽管PDI的氧化还原活性对各种生物过程至关重要,建议MTP的功能是不必要的。然而,这一结论从未在遗传模型中得到验证。此外,PDI家族有20多个成员,其中大多数与PDI显示出非常相似的序列、结构和功能。尽管PDI是MTP活性所必需的,但其他PDI旁系同源物(PDI)是否在维持肝内和血浆脂质稳态中发挥特异性或冗余作用仍然难以捉摸。
在本研究中,基于对ER应激与SFA和UFA不同转运机制相关的观察,研究者使用肝细胞特异性和全身基因缺陷小鼠模型筛选了PDI家族的13名成员,并确定只有PDI在调节肝内和血管内脂质稳态中起着不可或缺且不可替代的作用。进一步的研究表明,PDI对于将UFA酯转移出肝脏至关重要,但SFA酯则不重要。此外,PDI催化MTP的氧化折叠,负责形成至少3个二硫键,这对MTP的结构稳定性非常重要。肝细胞中的PDI缺陷消除了ApoB-100VLDL分泌,同时维持了ApoB-48VLDL的部分分泌。这些发现促进了对脂肪酸转运原理的理解,并可能有助于开发治疗肝脂肪变性、低脂血症和肥胖的新型治疗策略。
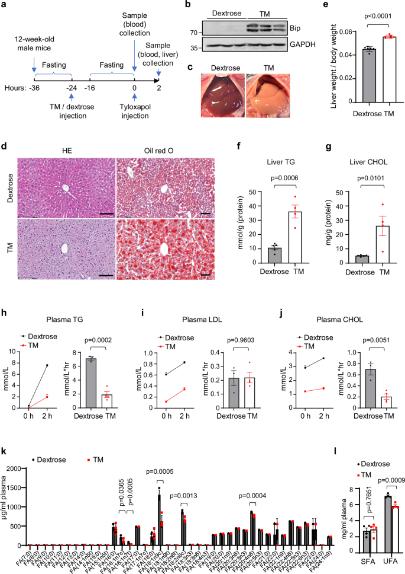
图1 ER应力与UFA和SFA酯的差异传递有关(摘自Nature communications )
参考消息:
https://doi.org/10.1038/s41467-025-56620-4
来源:iNature
- 随机文章
- 热门文章
- 热评文章
- 入市新动向!理财公司积极布局此类产品
- 一针即可安全显著降低HBsAg!全球首个慢乙肝基因编辑疗法PBGEN
- 山东民营企业家:坚定信心,做大做优做强民营企业
- 1006个重大项目、10427亿元总投资……这个会描出2025山东春忙图
- 校长曾良凌晨逝世,年仅54岁,年初还在上思政课
- 漫山雾凇挂枝头
- 游客在西岭雪山偶遇野生小熊猫引发网友关注!景区:将持续关注
- 春运期间新疆机场集团旅客吞吐量5346万人次较2024年春运同期














 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号