iNature
在TME中募集多形核MDSC(PMN-MDSC)抑制肿瘤浸润CD8+ T细胞(CD8+ TILs)的抗肿瘤活性。然而,对于抗肿瘤CD8+ TILs在影响免疫耐受微环境中的作用,尤其是在PMN-MDSC的募集中,仍知之甚少。
2025年2月5日,南京大学董杰及魏继武共同通讯在Cellular & Molecular Immunology 在线发表题为“GLP1 alleviates oleic acid-propelled lipocalin-2 generation by tumor-infiltrating CD8+?T cells to reduce polymorphonuclear MDSC recruitment and enhances viral immunotherapy in pancreatic cancer”的研究论文。该研究发现免疫治疗激活的CD8+ TILs增加了TME中PNM-MDSC的浸润,导致抗肿瘤耐药。
当CD8+ T细胞被激活时,脂质运载蛋白-2(LCN2)表达上调,增强PMN-MDSC趋化性。从机制上讲,免疫激活增加了CD8+ T细胞中的脂肪酸合成,特别是油酸(OA),诱导溶酶体膜通透性,释放组织蛋白酶B,随后激活NF-κB以促进LCN2表达。此外,作者发现胰高血糖素样肽1(GLP1)有效抑制活化CD8+ T细胞中的OA合成,减少LCN2的产生。作者开发了一种编码GLP1(AdV-GLP1)的重组腺病毒,显著减少了PMN-MDSC浸润并恢复了CD8+ TILs的抗肿瘤活性。在各种胰腺癌模型中(包括皮下、原位和人源化CDX/PDX模型),AdV-GLP1表现出优异的抗肿瘤疗效。该研究加深了对免疫疗法激活的CD8+ TILs如何诱导PMN-MDSC浸润的理解,提供了针对这种相互作用和改善癌症免疫治疗效果的临床相关策略。

细胞毒性CD8+ T细胞是参与抗肿瘤免疫的主要效应免疫细胞,其浸润、定位和激活与许多实体瘤的预后密切相关。然而,肿瘤微环境(TME)的复杂性决定了抗肿瘤免疫治疗的结果,包括CD8+ T细胞与肿瘤细胞以及其他免疫细胞(如髓源性抑制细胞(MDSC)、肿瘤相关巨噬细胞(TAM)和调节性T细胞)之间的相互作用。
MDSC在许多实体瘤的TME中大量存在,是源自未成熟髓系细胞的异质性群体,分为两个主要亚群:粒细胞或多形核(PMN-MDSC)和单核细胞(M-MDSC)。MDSCs可以通过多种机制诱导T细胞凋亡并抑制CD8+ T细胞的增殖和扩增,从而在肿瘤免疫逃逸和治疗耐药中发挥关键作用。然而,CD8+ T细胞和MDSCs之间的相互作用应该是双向的。迄今为止,仍对CD8+ T细胞的作用知之甚少,尚未有研究报道针对这种相互作用来提高抗肿瘤效果的策略。
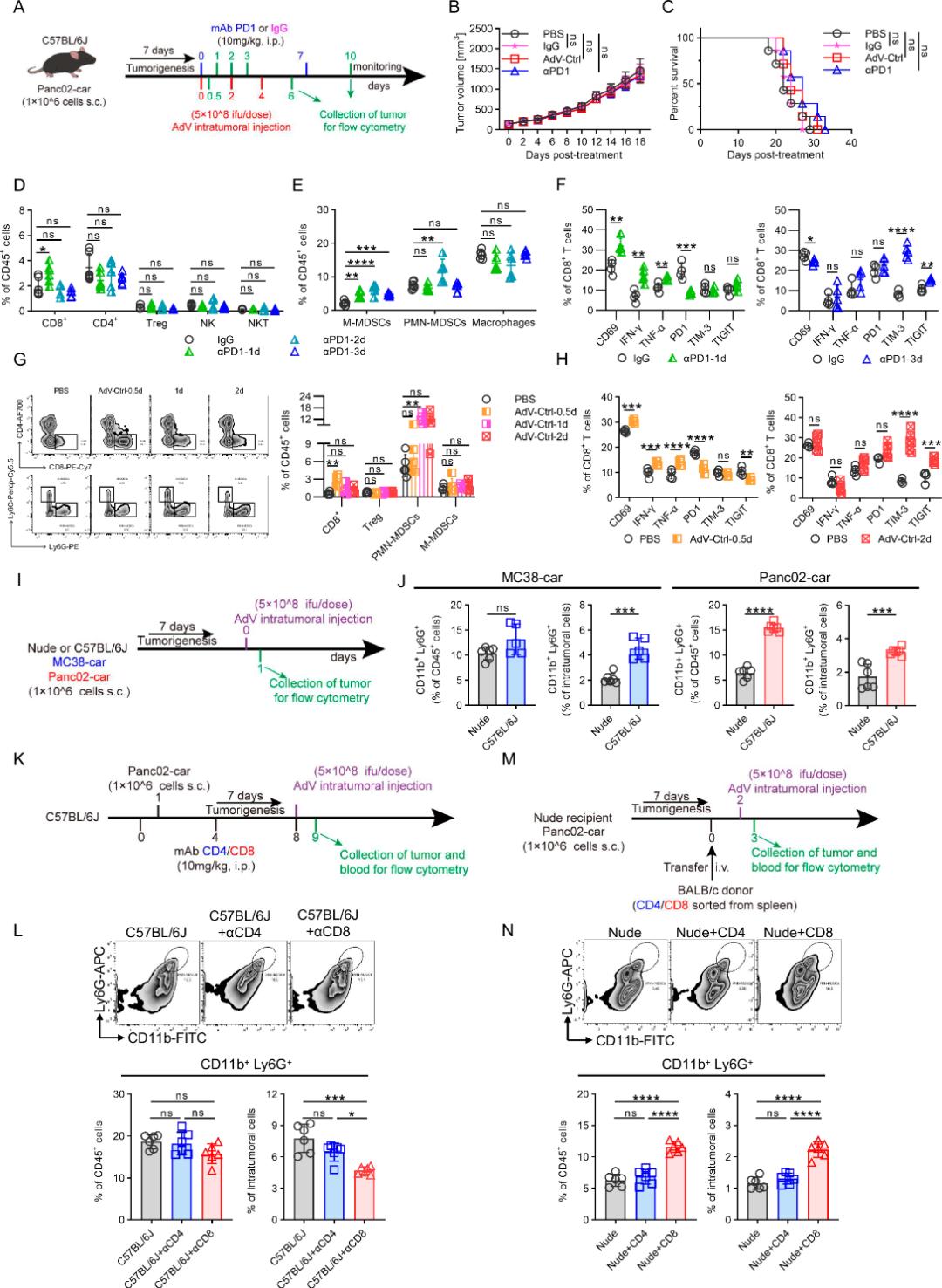
图1 CD8+ T细胞有助于TME中PMN-MDSC的浸润(摘自Cellular & Molecular Immunology )
激活后,CD8+ T细胞发生代谢适应,与核苷酸、氨基酸和脂肪酸(FA)合成的合成代谢途径相关的代谢物急剧增加。值得注意的是,FA从头合成在T细胞活化中尤为重要。脂肪酸代谢在肿瘤浸润CD8+ T细胞(CD8+ TILs)的抗肿瘤过程中发挥的作用存在争议。据报道,CD8+ T细胞中FA氧化的增加会损害其抗肿瘤反应。相反,一些报告显示,足量的FA对于满足CD8+ T细胞的能量需求、提高其抗肿瘤功效至关重要。此外,不同的FA代谢物可能在CD8+ T细胞中发挥的作用相反。最近的一项研究报道,油酸(OA)改善了棕榈酸(PA)导致的CD8+ T细胞线粒体代谢减弱,维持其杀伤活性。相反,另一项研究表明,SCD1抑制剂可降低CD8+ T细胞中的OA和酯化胆固醇,导致IFN-γ产生和细胞毒性增加。当前,尚不清楚OA对CD8+ T细胞的影响,尤其是OA与其他免疫细胞(如MDSC)的相互作用。
溶瘤病毒(OVs)是一类能够在肿瘤细胞中自我复制和选择性复制,导致细胞裂解和死亡的病毒。除了固有的溶瘤作用外,其抗肿瘤功效主要取决于诱导抗肿瘤免疫的能力。OVs通过溶瘤释放肿瘤相关抗原和一系列危险信号,包括损伤相关分子模式(DAMPs)和病原体相关分子模式(PAMPs),从而诱导免疫原性细胞死亡(ICD)。此外,作为外来微生物入侵者,OVs有效刺激免疫细胞浸润,促进肿瘤细胞识别和攻击,将肿瘤从“冷”转变为“热”。腺病毒是一种无包膜的双链线性DNA病毒,有52种已知的人类血清型。其中,E1B-55kD基因突变的5型腺病毒在肿瘤细胞中选择性复制,产生直接的溶瘤作用,诱导抗肿瘤免疫,并表现出高安全性。
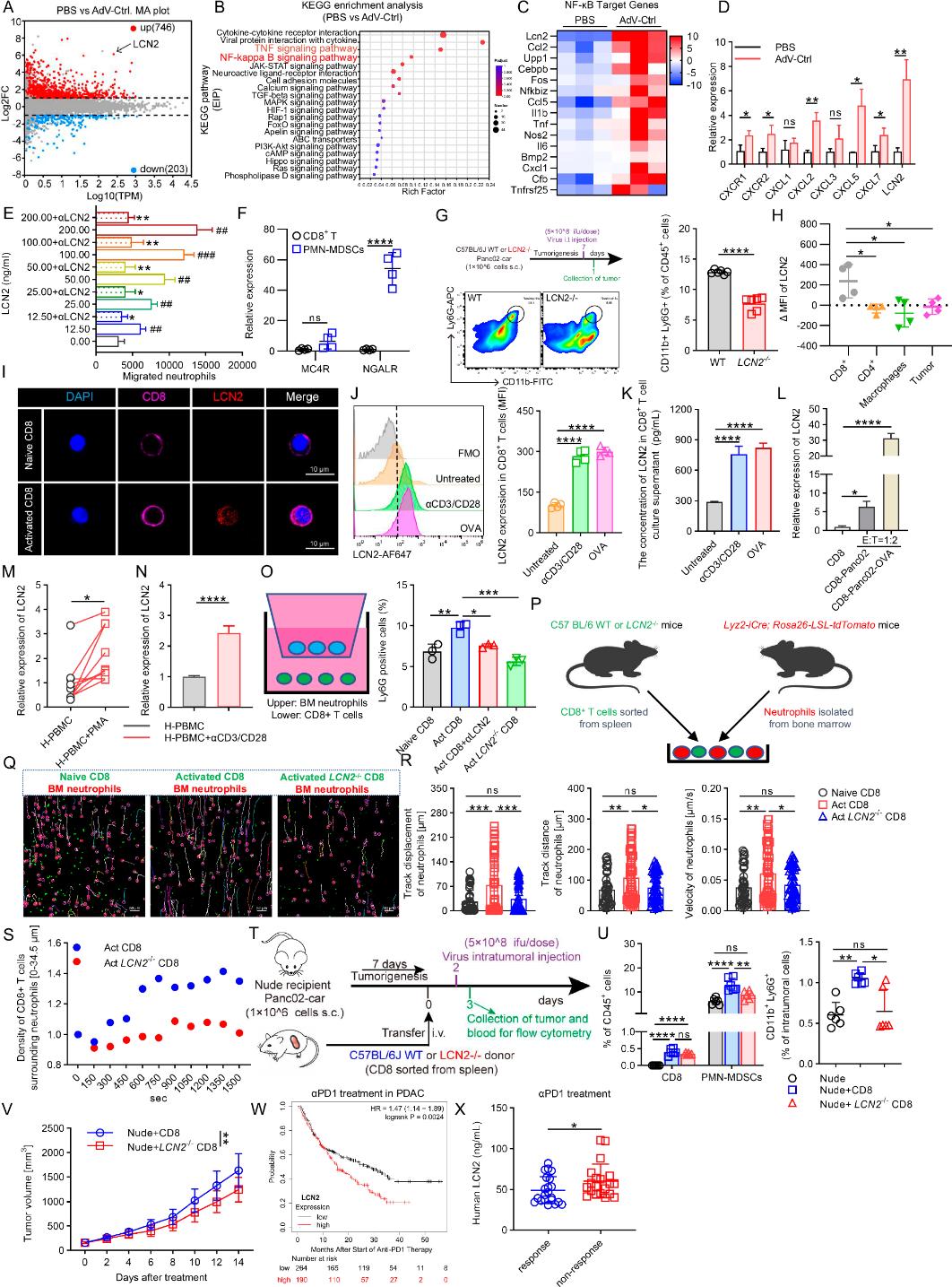
图2 CD8+ T 细胞产生的LCN2参与PMN-MDSC的趋化性(摘自Cellular & Molecular Immunology )
该研究探索了胰腺癌小鼠模型中,免疫治疗激活的CD8+ TILs在PMN-MDSCs募集到TME过程中发挥的作用,阐明了重编程OA如何促进CD8+ T细胞转化为趋化性PMN-MDSC。作者还研究了胰高血糖素样肽1(GLP1)在调节CD8+ T细胞OA代谢中的作用,并设计了一种编码GLP1(AdV-GLP1)的重组溶瘤腺病毒来调控TME中CD8+ TILs的OA代谢。该研究揭示了抗肿瘤CD8+ TILs在免疫抑制性微环境中未明确的作用,首次提供了一种临床相关疗法,通过AdV-GLP1原位阻断,在癌症免疫治疗中实现更好的抗肿瘤结果。
参考消息:
https://www.nature.com/articles/s41423-025-01260-3
来源:iNature
- 随机文章
- 热门文章
- 热评文章
- 仅55小时,立春以来贵阳平均日照时数为何偏少?
- 申进科回应女中学生好奇轰炸机:知道我也不能说!
- 美胁迫别国打压我半导体产业,外交部:损人害己!
- 2024年环县首创了一批示范推广的环县模式
- 环县环城初中:上好开学第一课开启美好新学期
- 今天起,可以查分了!
- 南京师范大学通报:教师宋某某涉嫌师德失范,免去环境学院副院
- 聚焦一线宝鸡市一平台三措施工作模式有效解决电动自行车安全














 京公网安备11000000000001号
京公网安备11000000000001号 京ICP备11000001号
京ICP备11000001号